【通讯员:庞家栋】2025年3月,南方科技大学医院创新研究院庞家栋博士在《Journal of Controlled Release》(中科院1区Top,影响因子10.5)以第一作者身份在线发表题为《Inhalable pH-responsive charge-reversal polymer-small interfering RNA polyplexes for directed gene therapy of anaplastic lymphoma kinase fusion-positive lung cancer》研究性论文。中山大学肿瘤医院杨江研究员为论文通讯作者。

间变性淋巴瘤激酶(ALK)致癌融合基因是非小细胞肺癌(NSCLC)中ALK融合阳性(ALK+)肿瘤的一个臭名昭著且不断演变的靶点。RNA干扰(RNAi)是小分子ALK抑制剂的一种潜在替代疗法,但其存在细胞递送效果差和稳定性低的问题,这限制了其持续的靶向治疗效果。为了在肺部靶点实现非侵入性的直接RNAi,需要可吸入载体来保护不稳定的siRNA免受碱性胸腔积液的降解,并在酸性肿瘤微环境中递送siRNA。在此,我们通过化学合成了一种通用的聚乙二醇-聚(β-氨基酯)-组氨酸(PEG-PBAE-His,PPH)系统,该系统能够实现对ALK+ NSCLC中ALK基因的siRNA定向沉默,并具有可控释放功能。聚乙二醇化的聚阳离子PPH的合理设计将聚乙二醇冠层的非离子性、惰性、隐身效应和低免疫原性与双正电荷的PBAE和His相结合,通过增强的静电复合来封装siRNA负载物。所组装的低多分散性的聚复合物在碱性胸腔积液中整体呈阴离子性。38 在酸性 pH 值条件下,该物质会从流体状态转变为阳离子电荷,从而促进细胞摄取,并在溶酶体 pH 值控制下释放。这种由 PPH 引导的递送显著提高了 siRNA 的稳定性,并在 H3122 细胞中实现了 ALK 序列特异性敲低,其转染效率与商业聚乙烯亚胺相当,但细胞毒性更低。这种以 ALK 为中心的 RNAi 疗法通过吸入方式,可抑制 ALK+非小细胞肺癌异种移植瘤的克隆形成、迁移和侵袭,并诱导其生长受到显著抑制。这种可吸入的聚复合物代表了一种变革性的递送平台,它结合了pH响应性靶向、增强的稳定性和低毒性,解决了现有 siRNA 递送系统的关键局限性。
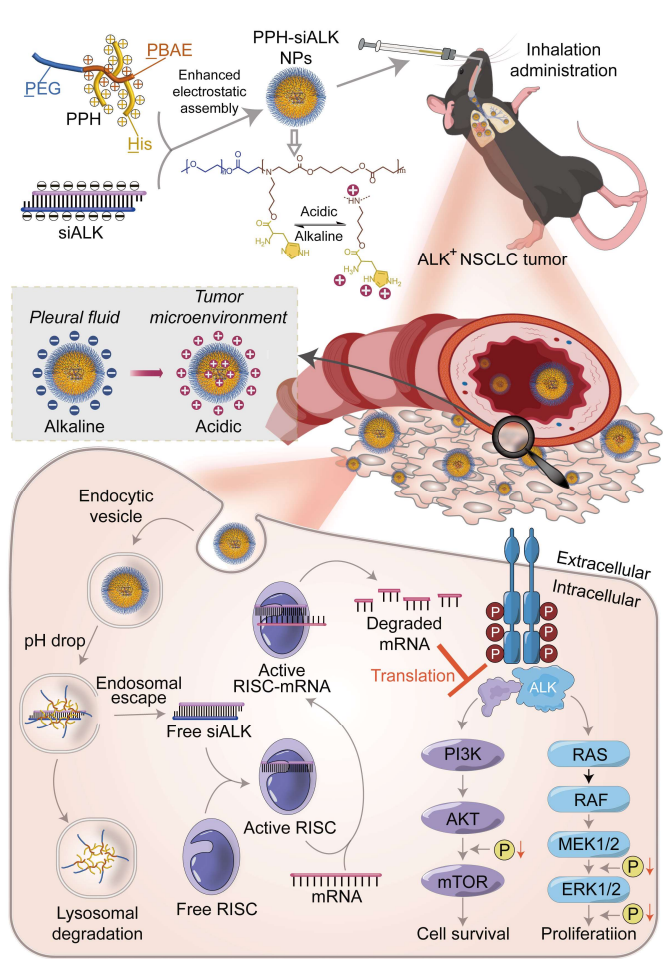
图1.通过双正电荷的 PBAE 和 His 增强电荷反转的 PPH-siALK 多聚复合物的静电共组装,实现针对 ALK+非小细胞肺癌的 siRNA 指导的吸入式 ALK 基因沉默。
研究亮点
(1)pH响应电荷反转递送系统:开发了PEG-PBAE-His(PPH)聚合物,该聚合物在碱性胸膜液中呈阴离子以保护siRNA,而在酸性肿瘤微环境中转变为阳离子,增强细胞摄取和溶酶体逃逸,实现精准控释。
(2)高效基因沉默与低毒性:通过分子动力学模拟和实验验证,PPH与siRNA形成稳定复合物,体外转染效率媲美商业PEI但毒性更低。体内实验显示,吸入PPH-siALK显著抑制ALK+肺癌生长(肿瘤抑制率84.5%),并下调MAPK/PI3K-AKT信号通路。
(3)非侵入性吸入给药策略:首次实现siRNA的吸入式递送,药代动力学表明药物主要富集于肺部,减少全身暴露。呼吸功能测试证实治疗改善肺通气,且血液学与组织学评估显示优异生物安全性,为肺癌靶向治疗提供新范式。
本研究在构建首个用于肺部给药的siRNA吸入递送平台方面取得突破性进展。药代动力学研究表明治疗药物主要富集于肺部,且系统暴露量显著降低。肺功能检测显示治疗后肺泡通气效率显著提升,综合血液学分析与组织病理学评估进一步证实了优异的生物安全性特征。该策略通过局部核酸靶向递送,为肺癌精准治疗建立了开创性范式。
该工作第一作者南方科技大学医院创新研究院庞家栋博士和东莞市人民医院陈晓瑜博士,中山大学肿瘤医院杨江研究员为论文通讯作者,南方科技大学医院为第二单位。庞家栋博士自进入医院开展工作以来,一直从事肿瘤显影与治疗相关纳米材料的研究,此前已于2023年和2024年在《International Journal of Biological Macromolecules》(中科院1区,IF 8.2)上陆续发表两篇基因与药物载体的研究型论文,此次为创新研究院第一篇10分以上高水平文章。该工作得到了国家自然科学基金(82472041、82071978 和 52271196)、中国博士后科学基金(2019M653217)以及广州市科技计划项目(2023A04J2128)等项目的支持。
原文链接:http://doi.org/10.1016/j.jconrel.2025.113644